Fístula nasal de líquido cefalorraquídeo post-traumática. Resultados de la implementación de un protocolo de trabajo.
Liezel Ulloque Caamaño,1 Juan F. Villalonga,2 Alexander J. Zúñiga,1
Benjamín Romero-Leguina,1 Luis F. Aiquel,3 Álvaro Campero2
1. Residencia de Neurocirugía Hospital Ángel C. Padilla, Tucumán, Argentina
2. LINT, Facultad de Medicina, Universidad Nacional de Tucumán, Tucumán, Argentina.
3. Servicio de Neurocirugía Hospital Ángel C. Padilla, Tucumán, Argentina
Liezel Uloque Caamaño
liucax@hotmail.com
Recibido: febrero de 2023. Aceptado: marzo de 2023.
DOI: 10.59156/revista.v37i02.495
ORCID:
Liezel Ulloque-Caamaño: 0000-0002-3973-3813
Alexander J. Zúñiga:009-0006-9094-5906
Alejandro B. Romero Leguina:009-0008-4535-6939
Juan F. Villalonga:0000-0002-1544-6334
Luis F. Aiquel:009-0000-1395-9286
Álvaro Campero:0000-0001-5184-5052
RESUMEN
Introducción: Los pacientes con fracturas de base de cráneo anterior post traumatismo encéfalo-craneano tienen alto riesgo de fístula de líquido céfalo-raquídeo por las fosas nasales. Es importante el manejo oportuno y apropiado, evitando así complicaciones; razón por la cual se desarrolló el “protocolo HP” para su tratamiento quirúrgico.
Objetivo: Comunicar la utilidad del “protocolo HP” en el manejo de la fístula de líquido céfalo-raquídeo de la base de cráneo anterior.
Materiales y métodos: Estudio transversal retrospectivo con pacientes ≥ 15 años con diagnóstico de fístula de líquido céfalo-raquídeo nasal post traumatismo encéfalo-craneano, desde 1/1/2016 hasta 31/8/2021 que ingresaron al hospital y requirieron cirugía de reparación, con 28 pacientes incluidos, el valor p ˂0,05 (estadísticamente significativo).
Resultados: 96,4% hombres, mayoría adultos jóvenes con traumatismo encéfalo-craneano leve; 82,1% presentó fístula de líquido céfalo-raquídeo temprana. Todos requirieron reparación transcraneal frontal, en 67,9% fue bilateral. La reparación antes de los 7 días fue en el 39,3%, 7-21 días en 46,4% y después de 21 días en 14,3% de los casos. Uso de drenaje lumbar continuo: preoperatorio 10,7%, intraoperatorio 60,7%, postoperatorio 46,4%. En el 89,3% la ubicación de la fístula de líquido céfalo-raquídeo intra-quirúrgica fue congruente con la tomografía. Desde el 2020 se sistematizó el manejo de las fístula de líquido céfalo-raquídeo. La recurrencia fue de 10,7% antes del 2020 (posteriormente fue de 0%), asociándose con Glasgow bajo e inicio de fístula de líquido céfalo-raquídeo 7 días post traumatismo encéfalo-craneano (p˂0,05). Complicaciones encontradas: meningitis 28,6%, convulsión 25%, anosmia 14,3%, neumoencéfalo a tensión 7,1% y absceso 3,6%. Mortalidad por fístula de líquido céfalo-raquídeo: 3,6%. Curación 96,4%.
Conclusiones: La aplicación del “Protocolo HP” tuvo resultados satisfactorios. La tasa de recurrencia postoperatoria de fístula de líquido céfalo-raquídeo nasal post traumatismo encéfalo-craneano fue 0%.
Palabras claves: Abordaje a la base de cráneo. Fístula de líquido cefalorraquídeo. Fractura de base de cráneo. Traumatismo encéfalo-craneano.
Post-traumatic cerebrospinal fluid nasal leak. Results of the implementation of a work protocol.
ABSTRACT
Background. Patients with anterior skull base fractures after traumatic brain injury have a high risk of cerebrospinal fluid leak through the nostrils. Timely and appropriate management is important, avoiding complications. The “HP protocol” for surgical treatment was developed.
Objectives. To communicate the utility of the “HP protocol” in the management of the anterior skull base cerebrospinal fluid leak.
Methods: Retrospective cross-sectional study; patients ≥ 15 years old with a diagnosis of nasal cerebrospinal fluid leak after traumatic brain injury, who were admitted at the hospital from 1/1/2016 to 8/31/2021 and required surgery. Included 28 patients, p value ˂0.05 (statistically significant).
Results: 96.4% men, mostly young adults with mild traumatic brain injury; 82.1% presented early cerebrospinal fluid leak. All required frontal transcranial repair, in 67.9% it was bilateral. Repair before 7 days was in 39.3%, 7-21 days in 46.4%, and after 21 days in 14.3%. Use of continuous lumbar drainage: preoperative 10.7%, intraoperative 60.7%, postoperative 46.4%. In 89.3%, the location of the intraoperative cerebrospinal fluid leak was consistent with the CT scan. Since 2020, the management of the cerebrospinal fluid leak was systematized. The recurrence was 10.7% before 2020; after it was 0% and associated with low Glasgow and onset of cerebrospinal fluid leak 7 days after traumatic brain injury (p<0.05). Complications: meningitis 28.6%, seizure 25%, anosmia 14.3%, high tension pneumocephalus 7.1% and abscess 3.6%. Cerebrospinal fluid leak mortality: 3.6%. Cure 96.4%.
Conclusions: The application of the “HP Protocol” had satisfactory results. The post traumatic brain injury nasal cerebrospinal fluid leak recurrence rate was 0%.
Keywords: Anterior skull base fracture. Cerebrospinal fluid leak. Skull base approach. Traumatic brain injury.
INTRODUCCIÓN
La fístula de líquido cefalorraquídeo (FLCR) es la comunicación del espacio subaracnoideo con el exterior a través de una brecha meníngea con fuga de LCR. Genera complicaciones como neumoencéfalo, meningitis y abscesos cerebrales.1 Según la causa pueden ser espontáneas, iatrogénicas y traumáticas.2
A nivel mundial, las FLCR postraumáticas se observan entre el 1% y el 3% de los traumatismos encéfalo-craneano (TEC) cerrados en adultos y el 80%-90% de todas las FLCR en pacientes adultos se deben a TEC.3,4
En la provincia de Tucumán son muy frecuentes los TEC con cinemáticas de alto impacto, en su mayoría por accidentes en moto sin casco bajo intoxicación etílica, convirtiéndose en un problema de salud pública. Solo en el año 2020 ingresaron al Hospital “Ángel C. Padilla” 5.196 pacientes con TEC; de éstos, el 0,2% (n:9) presentó FLCR nasal que no se autolimitó y requirió tratamiento quirúrgico transcraneano.
No existe en la literatura hispana protocolos actualizados para toma de decisiones en esta patología. Nuestro equipo sistematizó el manejo quirúrgico y perioperatorio, al cual hemos denominado “Protocolo HP” (i.e. Hospital Padilla). El objetivo del presente trabajo es comunicar la utilidad del protocolo HP en el manejo de las FLCR post-TEC de la fosa anterior.
MÉTODOS
Protocolo de trabajo
El protocolo HP incluye el manejo: preoperatorio, intraoperatorio y postoperatorio de pacientes con FLCR post-TEC que se realiza en el Hospital Ángel C. Padilla.
Manejo general y específicas de pacientes con FLCR nasal
Estas medidas buscan limitar la FLCR, evitando cirugía en pacientes con FLCR de bajo débito, que aparece solo al esfuerzo, con fracturas pequeñas y/o únicas.
Manejo preoperatorio
Vacunas
Aplicar vacunas antineumocócica y antimeningocócica, disminuyendo el riesgo de meningitis por estos gérmenes.
Medidas generales
Para disminuir la presión intracraneana se indica: reposo absoluto, cabecera a 30°, dieta rica en fibra, laxantes e hidratación. Si con 48 horas de medidas generales persiste la FLCR, se continua con las medidas específicas.
Medidas específicas
Reducen la cantidad de LCR, disminuyendo su producción con acetazolamida 250 mg cada 12 horas, o eliminándolo con drenaje lumbar continuo (DLC) por 5 a 7 días (en ausencia de neumoencéfalo).
Estas medidas se aplican de inicio si es una FLCR en reposo, de alto débito, o el trazo fracturario es grande o múltiple; si estas medidas no son exitosas, se indica reparación quirúrgica.
TC cerebral
TC 2D de encéfalo y macizo facial el día previo a la cirugía, con cortes óseos de 1 mm y reconstrucción ósea 3D, se evalúan cortes coronales y sagitales para la identificación de la brecha y estudiar el progreso de las lesiones asociadas (hematomas, contusión, edema).
Punción lumbar (PL)
El día previo a la cirugía para determinar si existe meningitis prequirúrgica.
Estrategia y momento quirúrgico
Definir conducta y momento de cirugía según tipo de fístula y regla 3x3. Definir la vía quirúrgica según clasificación Madhusudan y cols (Figura 1 y 2).1,2,7

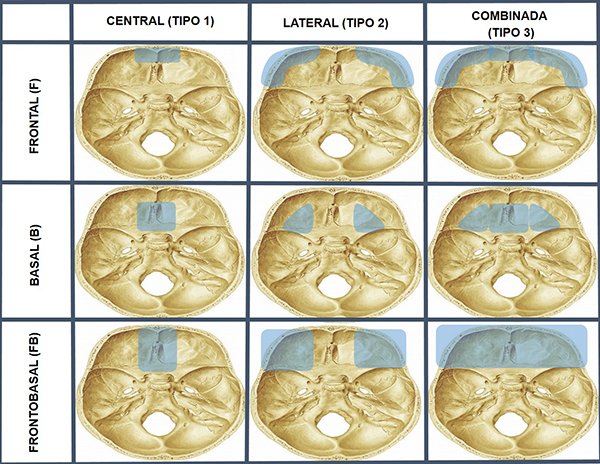
Figura 1. Clasificación de Madhusudan de las fracturas frontobasales. F1= Hueso frontal central, seno frontal, tercio medio de bordes orbitarios superiores. F2= Dos tercios lateral del borde orbitario superior, hueso frontal lateral y escama del temporal. B1= Nasoetmoidal, lamina cribiforme, planum esfenoidal. B2= Techo, pared lateral y ápice de la órbita. FB1= F1+B1. FB2= F2+B2. Combinada: F3= F1+F2, B3= B1+B2, FB3= FB1+FB2.
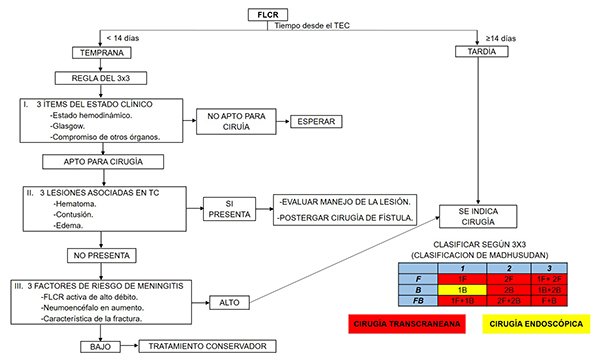
Figura 2. Algoritmo prequirúrgico.
Drenaje Lumbar Continuo (DLC)
En pacientes con persistencia de FLCR candidatos a cirugía de reparación, sin DLC previo, se coloca uno en el quirófano el día de la cirugía una vez sedado. En pacientes con DLC previo éste se mantiene abierto, con el fin de drenar máximo 90 ml de LCR durante el abordaje, para optimizar la relajación cerebral y disminuir el uso de espátulas de retracción.
Manejo intraoperatorio
Posición
Decúbito dorsal. Packing orofaríngeo. Cabezal de tres puntos. Tórax a 30 grados, cabeza en posición neutra. Protección de decúbitos, realce en hueco poplíteo. Miembro inferior izquierdo flexionado con rodilla al cenit, rotado 20 grados hacia medial, se fija con cinta adhesiva evitando recorrido del nervio ciático poplíteo externo a nivel de la rodilla. Se coloca arco (Figura 3).
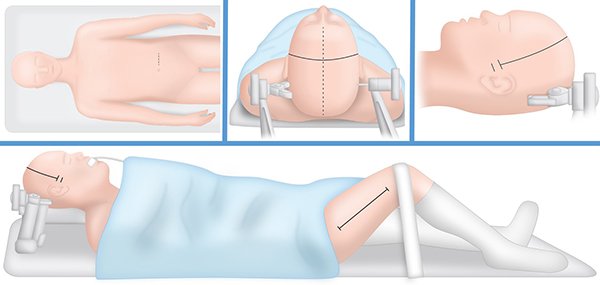
Figura 3. Posición, tricotomía y marcación.
Tricotomía y marcación
Tricotomía cefálica total. Protección ocular. Lavado profuso de cabeza, abdomen y muslo izquierdo con solución fisiológica y clorhexidina jabonosa seis veces. Con fibra indeleble se marca ambos cigomas y luego línea bicoronal en casos de trazo fracturario bilateral; en caso de trazo unilateral se marca una línea tres cuartos coronal ipsilateral. Se realiza marcación lineal a lo largo de la cara lateral del muslo de 10 cm y marcación lineal horizontal paraumbilical de aproximadamente 5 cm (Figura 3).
Colocación de campos
Se realiza asepsia con yodopovidona tres veces a nivel cefálico, abdomen y muslo. Se coloca campo estéril grande podálico a nivel supraciliar, dejando descubierta cara lateral del muslo y la mitad del abdomen reparado. Se coloca campo grande lateral cubriendo flanco abdominal, muslo y pierna reparada. Se colocan cuatro campos pequeños alrededor de la marcación cefálica, se fijan con puntos; se coloca campo grande en forma de babero a nivel cefálico, se procede a colocar cuatro compresas pequeñas alrededor de la marcación abdominal y el muslo reparado. Se cubre todo con campo quirúrgico adhesivo antimicrobiano. Se fijan campos al arco con una goma elástica rodeando parte inferior de cabezal, se coloca un campo telón podálico hacia el lado derecho del paciente. Se colocan cuatro compresas alrededor de marcación cefálica y sobre ésta, una bolsa estéril recolectora fenestrada, exponiendo así el campo cefálico y se cubre con campo quirúrgico adhesivo antimicrobiano de incisión.
Partes blandas
Con bisturí frio Nº 24, se realiza incisión bicoronal o tres cuartos coronal según sea el caso. Bicoronal: Incisión profunda hasta plano óseo uniendo la línea temporal superior (LTS) con su contralateral; desde LTS hasta el cigoma la incisión es más superficial hasta el tejido celular subcutáneo (TCS), con disección del plano muscular temporal con tijera Metzembaum. Se rebate flap de partes blandas en un plano, se exponen ambos arcos supraciliares. Desinserción de ambos músculos temporales con monopolar y exposición de keyholes. Se rebate mínimamente con anzuelos ambos músculos temporales hacia caudal. Con esto se logra una adecuada exposición del plano óseo (Figura 4). Tres cuartos coronal: en este caso la incisión se realiza hasta la línea medio pupilar contralateral del lado afectado, siendo el resto de los pasos idénticos, pero unilaterales.
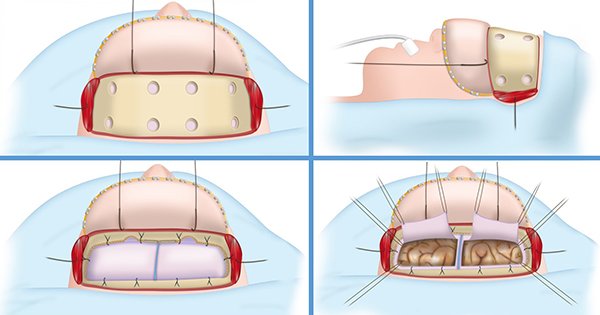
Figura 4. Tratamiento de partes blandas, craneotomia y durotomia.
Craneotomía
En pacientes con fracturas bilaterales se realiza craneotomía bicoronal mediante ocho orificios de trépano, cuatro anteriores y cuatro posteriores. Los cuatro anteriores: uno en keyhole derecho, uno en keyhole izquierdo, dos a ambos lados de seno longitudinal superior (SLS). Cuatro posteriores (aproximadamente a 4 cm de los orificios anteriores): uno en LTS izquierda, otro en LTS derecha, dos a ambos lados de SLS. Con disector tipo Penfield se realiza disección de duramadre. Con pasa sierra de Gigli, se chequea la adecuada disección dural desde un orificio hacia el otro. Craneotomía con craneótomo (Figura 4). En pacientes con fracturas unilaterales se realiza craneotomía unicoronal mediante cuatro orificios de trépano, dos anteriores y dos posteriores. Los dos anteriores: uno en Keyhole y uno al lado del SLS. Dos posteriores (también aproximadamente 4 cm de orificios anteriores): uno a nivel LTS, uno al lado de SLS.
Desfuncionalización del seno frontal
Consiste en la resección de pared posterior del seno frontal, coagulación minuciosa de la mucosa e identificación de los “ostiums”. Es un paso clave: la impactación de hueso autólogo en los “ostiums” hasta obturarlos. Se colocan cuatro algodones con cola embebidos en yodopovidona.
Durotomía
Se ancla duramadre a los rebordes óseos. Luego bajo visión microscópica con bisturí hoja N° 11 y tijera Metzembaum se realiza durotomía arciforme con base en la órbita unilateral o bilateral según corresponda, respetando un trayecto lineal de duramadre que recubra el SLS. Retracción dural con punto de seda 4-0 hacia el arco orbitario (Figura 4).
Ligadura de SLS
Ésta es rutinaria en casos en donde es necesario exponer ambos lóbulos frontales, se realiza en la mitad anterior del tercio anterior del SLS. Para proteger el cerebro se coloca en la cara interna borde de guante de látex y planchuela de algodón. Con punto de sutura de lino 30, se atraviesa la hoz cerebral y luego se liga. Se realizan dos ligaduras anteriores y dos posteriores, se coagula el SLS entre ambas ligaduras con bipolar y se corta en un punto equidistante de ambas ligaduras, prosiguiendo con la hoz cerebral hasta la base del cráneo (Figura 5).
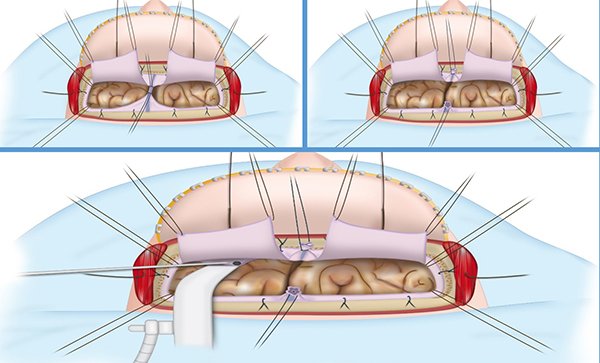
Figura 5. Ligadura del seno longitudinal superior e identificación de brecha fistulosa.
Segundos campos
Se colocan segundos campos azules cubriendo el borde de la craneotomía, éstos se fijan mediante tracción con Prolene 2.0, desde los rebordes durales hacia los campos fijados por la goma. Con esto, se evita que la sangre extradural invada el campo quirúrgico en la etapa microscópica.
Identificación de la brecha fistulosa
Bajo visión microscópica se coloca borde de guante de látex sobre superficie cerebral muchas veces edematizada. Planchuela de algodón sobre el primero, retracción anteroposterior con cánula sobre algodón. Si se requiere mayor relajación cerebral, se incide en cisterna interóptica sin utilizar espátula. Si es necesario se separa con algodón. Drenaje de LCR lento durante diez minutos, logrando relajación cerebral. Se opta la retracción cerebral con sistema de Leyla solo en casos específicos. Con disector curvo Nº 1 (Aesculap AR 5), se identifica la brecha fistulosa dural. Ante la presencia de encefalocele es necesaria su resección mediante coagulación bipolar, ya que no permite la identificación correcta de la brecha fistulosa en cuestión (Figura 5).
Tratamiento de la brecha fistulosa
Disección de la duramadre del área fistulosa hasta identificar brecha ósea. Se impacta hueso autólogo en la brecha. En caso de fracturas lineales, en las que no se puede impactar hueso, se coloca músculo libre con un disector para la obturación de la brecha y, en casos de defectos muy grandes, se coloca malla de titanio. Se tapiza la reparación con injerto libre de fascia lata autóloga y se sutura la misma con puntos de Prolene 5-0 (Covidien Surgipro 2 CV-22) al borde dural sano. Control de hemostasia en durorrafia ya que generalmente, la duramadre basal remanente sangra. Se coloca cola de fibrina en bordes de tapizado (Beriplast) e injerto graso en bloque. Se comprueba hemostasia con Maniobra de Valsalva. Surgicel sobre superficie cerebral. Cierre dural hermético con puntos Surget simple de seda 4-0. Se revisa plano extradural en busca de fístula. En caso factible puede reforzarse el cierre intradural. Nueva valsalva para chequear hermetismo dural (Figura 6 y 7).
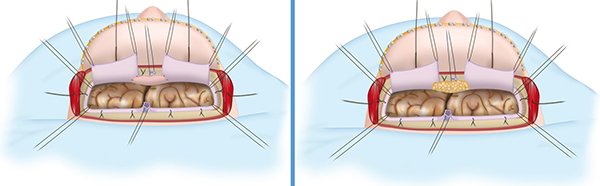
Figura 6. Tratamiento de la brecha fistulosa.
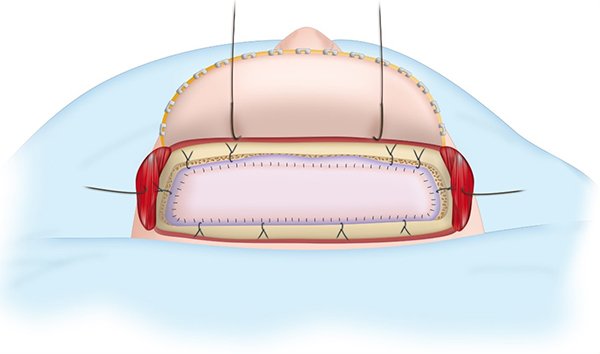
Figura 7. Duroplastia.
Cierre
Se procede a realizar agujeros en bordes de plaqueta y de craneotomía para su recolocación y fijación con Prolene 3-0. Se cubre entrada de ostium y seno frontal con músculo temporal pediculizado y se fija con Vicryl 3-0 con puntos simples a tejido celular subcutáneo y hueso. Se realiza hemostasia y lava con abundante suero fisiológico. Cierre de tejido celular subcutáneo con puntos simples con Vicryl 0 y de piel con puntos Surget cruzado con mononylon 3-0.
Manejo postoperatorio
Requerimiento de Unidad de Terapia Intensiva (UTI)
Por la complejidad quirúrgica, requiere cuidado neurocrítico postoperatorio, además, que suelen tener lesiones asociadas en otros órganos.
DLC
Queda cerrado por 24 horas, en ausencia de fístula, se retira. Si presenta queda con la cámara a nivel de la columna lumbar, drenando máximo 100 ml de LCR/ día hasta su cese, máximo 7 días.
TC cerebral
TC cerebral estándar a las 24 horas postoperatorio para identificar complicaciones de resolución quirúrgica inmediata.
PL
Si el paciente presenta 2 registros mayores a 38 grados, se realiza PL para descartar meningitis.
Reposo, bipedestación y deambulación
Reposo absoluto en cama por 3 días. En ausencia de fístula y si las condiciones lo permiten, debe comenzar a sentarse y deambular.
Alta
Tras 48 horas deambulando y sin fístula, se da alta hospitalaria.
Seguimiento
Seguimiento de herida y fístula cada 48 horas hasta el día 14 postoperatorio. Al día 21 se retiran puntos de sutura. Controles de la FLCR a los 3, 6 y 12 meses postquirúrgico. Tras 12 meses postquirúrgico sin FLCR, meningitis, absceso ni neumoencéfalo, se considera curación.
Pacientes operados
Estudio transversal retrospectivo, incluyéndose pacientes ≥ 15 años operados en el Hospital “Ángel C. Padilla” con diagnóstico de fístula nasal post-TEC, desde el 1 de enero del 2016 hasta el 31 de agosto del 2021. Se excluyeron a los pacientes con: fístula post-TEC no nasales (óticas u oculares), nasales post-TEC autolimitadas, espontáneas e iatrogénicas (posterior a cirugía transnasal, transesfenoidal u otorrinolaringológica).
Durante el periodo estudiado 25.234 pacientes ingresaron a la guardia por TEC, de los cuales 564 pacientes presentaron fractura de base de cráneo anterior con FLCR nasal; de éstos se autolimitó la fístula en 536 pacientes, requiriendo 28 pacientes cirugía de reparación, siendo incluidos en el presente estudio.
Se registraron datos demográficos, antecedentes personales, mecanismos del TEC, estado neurológico al ingreso y postquirúrgico, estudios radiológicos preoperatorios y postoperatorios, tiempo entre el TEC y la aparición de la fístula, conducta terapéutica, recurrencia y complicaciones. Los datos fueron obtenidos de la historia clínica digitalizada, interrogatorio y protocolos quirúrgicos.
El estado neurológico al ingreso se clasificó según la escala de coma de Glasgow,5 y alejado con la escala de Glasgow de la evolución (Glasgow outcome scale- GOS).6
Las tomografías pre y postoperatorias fueron protocolizadas: encéfalo y macizo facial con reconstrucción 2D en planos sagital y coronal, con cortes finos de 1 mm en ventana ósea y reconstrucción 3D.
Las FLCR fueron clasificadas en temprana, con aparición previa a los 14 días desde el TEC, y tardía, cuando se presentó luego de este periodo.2
Se clasificó la localización de las FLCR de acuerdo a la Clasificación de Madhusudan de las fracturas frontobasales (Figura 1).1,7
Los autores establecieron FLCR de bajo débito a aquella fístula que aparece como salida de LCR en gotas con un periodo de 15 segundos o más entre cada una (≤ a 4 gotas/minuto) con los cambios de posición y valsalvas, y FLCR de alto debito aquella que aparece como salida de LCR en gotas con un periodo de menos de 15 segundos entre cada una (≥ a 5 gotas/minuto) o salida continua con cambios de posición, valsalva o en reposo.
En cada caso, se registró el tratamiento elegido en base al protocolo de manejo preoperatorio y las cirugías estuvieron a cargo del mismo neurocirujano Senior (i.e. Luis Aiquel, encargado de dicha sección).
El análisis estadístico fue realizado con EPI INFO 7.2. Los datos cuantitativos no presentan distribución normal y se expresan en mediana (Me), y los cualitativos en porcentajes con sus intervalos de confianza al 95%. Las diferencias porcentuales se evaluaron con χ2, las medianas por el método de Kruskal-Wallis. Un valor de p<0.05 es estadísticamente significativo.
RESULTADOS
Los resultados obtenidos al analizar diversos aspectos de la presente serie de pacientes se presentan en las Tablas 1 a 11 y Gráficos 1 a 4.Tabla 1. Epidemiología.
| Me | |
| Edad | 26,5 años |
| n (%) | |
| Sexo | |
| Hombre | 27 (96,4%) |
| Mujer | 1 (3,6%) |
| Uso de drogas recreativas | 5 (17,9%) |
| Consumo de alcohol | 25 (89,3%) |
Tabla 2. Características del TEC.
| n (%) | |
| Mecanismo del TEC | |
| Accidente en moto sin casco | 26 (92,9%) |
| Herida por arma de fuego autoinfligida | 2 (7,1%) |
| Tipo del TEC | |
| Leve | 15 (53,6%) |
| Moderado | 4 (14,3%) |
| Grave | 9 (32,1%) |
Tabla 3. Otras lesiones en tomografía cerebral de ingreso.
| n (%) | |
| Presencia | |
| Si | 28 (100%) |
| No | 0 |
| Cantidad | |
| Única | 3 (10,7%) |
| Más de una | 25 (89,3%) |
Tabla 4. Características de la fractura.
| n (%) | |
| Sitio de fractura al ingreso | |
| Frontoetmoidal | 15 (53,6%) |
| Frontoesfenoetmoidal | 9 (32,1%) |
| Frontotemporoetmoidal | 2 (7,1%) |
| Frontal | 1 (3,6%) |
| Frontotemporoesfenoetmoidal | 1 (3,6%) |
| Me | |
| Área de la base de cráneo anterior (mm2) | 3.747,90 |
| Área de la fractura de la base de cráneo anterior (mm2) | 374,1 |
| Porcentaje del área de la base de cráneo anterior ocupado por la fractura (%) | 10,1 |
| n (%) | |
| Intervalo del porcentaje del área de la base de cráneo anterior ocupado por la fractura (%) | |
| ˂ 10 | 13 (46,4%) |
| 10 a 20 | 12 (42,9%) |
| ˃ 20 | 3 (10,7%) |
Tabla 5. Timming de manejo preoperatorio
| n (%) | |
| Tipo de fístula | |
| Temprana | 22 (78,6%) |
| Tardía | 6 (21,4%) |
| Tiempo desde el TEC hasta inicio de FLCR | |
| 0 días | 13 (46,4%) |
| 1-7 días | 7 (25%) |
| ˃ 7 días | 8 (28,6%) |
| Días desde el diagnóstico hasta la cirugía | |
| ˂ 7 días | 11 (39,3%) |
| 7-21 días | 13 (46,4%) |
| ˃21 días | 4 (14,3%) |
Tabla 6. Manejo de la FLCR.
| n (%) | |
| Uso de DLC | |
| Preoperatorio | 3 (10,7%) |
| Intraoperatorio: | |
| 1ra cirugía de reparación | 17 (60,7%) |
| 2da cirugía (Re intervención) (n=3) | 1 (33,3%) |
| Postoperatorio: | |
| 1ra cirugía de reparación | 13 (46,4%) |
| 2da cirugía (Re intervención) (n=3) | 0 |
| Posición quirúrgica | |
| Decúbito supino con cabeza en posición neutra | 28 (100%) |
| Otras | 0 |
| Abordaje quirúrgico | |
| Unilateral | 9 (32,1%) |
| Bilateral | 19 (67,9%) |
| Ligadura del seno sagital | 14 (50,0%) |
Tabla 7. Recurrencia de FLCR
| n (%) | |
| Recurrencia de la FLCR | 3 (10,7%) |
| Días desde la cirugía hasta la recurrencia de la FLCR | |
| ˂ 21 días | 1 (33,3%) |
| ≥21 días | 2 (66,7%) |
| Número de re cirugías necesarias para reparación de FLCR | |
| Una | 2 (66,7%) |
| Dos | 0 |
| Tres | 0 |
Tabla 8. Morbimortalidad
| n (%) | |
| Meningitis | 8 (28,6%) |
| Crisis comiciales | 7 (25,0%) |
| Anosmia | 4 (14,3%) |
| Neumoencéfalo a tensión | 2 (7,1%) |
| Absceso | 1 (3,6%) |
| Lesión vascular quirúrgica | 0 |
| Muerte | 2 (7,1%) |
Tabla 9. Recurrencia de FLCR según diversos factores.
| Si | No | P | |
| n=3 | n=25 | ||
| Glasgow | |||
| 3 | 2 (66,7%) | 1 (33,3%) | |
| 7 | 0 | 6 (100%) | |
| 9 | 0 | 1 (100%) | |
| 12 | 1 (33,3%) | 2 (66,7%) | 0,02*† |
| 13 | 0 | 4 (100%) | |
| 14 | 0 | 9 (100%) | |
| 15 | 0 | 2 (100%) | |
| Clasificación de la fractura | |||
| F2 | 0 | 1 (100%) | |
| FB1 | 1 (25,0%) | 3 (75,0%) | 0,7* |
| FB2 | 0 | 1 (100%) | |
| FB3 | 2 (9,1%) | 20 (90,9%) | |
| Porcentaje del área de la base anterior afectada | |||
| ˂ 10 | 1 (7,7%) | 12 (92,3%) | |
| 10 a 20 | 1 (8,3%) | 11 (91,7%) | 0,4* |
| ˃ 20 | 1 (33,3%) | 2 (66,7%) | |
| Tiempo desde el TEC hasta inicio de FLCR | |||
| 0 días | 0 | 13 (100%) | |
| 1-7 días | 0 | 7 (100%) | 0,015*† |
| ˃ 7 días | 3 (37,5%) | 5 (62,5%) |
*Chi cuadrado
†Estadísticamente significativo
Tabla 10. Presencia de neumoencéfalo según porcentaje del área de base anterior ocupado por la fractura.
| Intervalo del porcentaje del área de la base de cráneo anterior ocupado por la fractura (%) | Si | No | p |
| n=17 | n=11 | ||
| ˂ 10 | 9 (69,2%) | 4 (30,8%) | |
| 10 a 20 | 7 (58,3%) | 5 (41,7%) | 0,5* |
| ˃ 20 | 1 (33,3%) | 2 (66,7%) |
*Chi cuadrado
Tabla 11. Presencia de neumoencéfalo a tensión según porcentaje del área de base anterior ocupado por la fractura.
| Intervalo del porcentaje del área de la base de cráneo anterior ocupado por la fractura (%) | Si | No | p |
| n=2 | n=26 | ||
| ˂ 10 | 0 | 13 (100%) | |
| 10 a 20 | 1 (8,3%) | 11 (91,7%) | 0,1* |
| ˃ 20 | 1 (33,3%) | 2 (66,7%) |
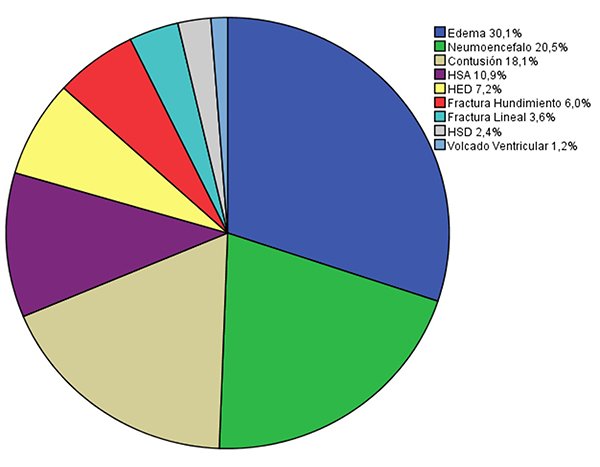
Gráfico 1. Otras lesiones en tomografía cerebral de ingreso.
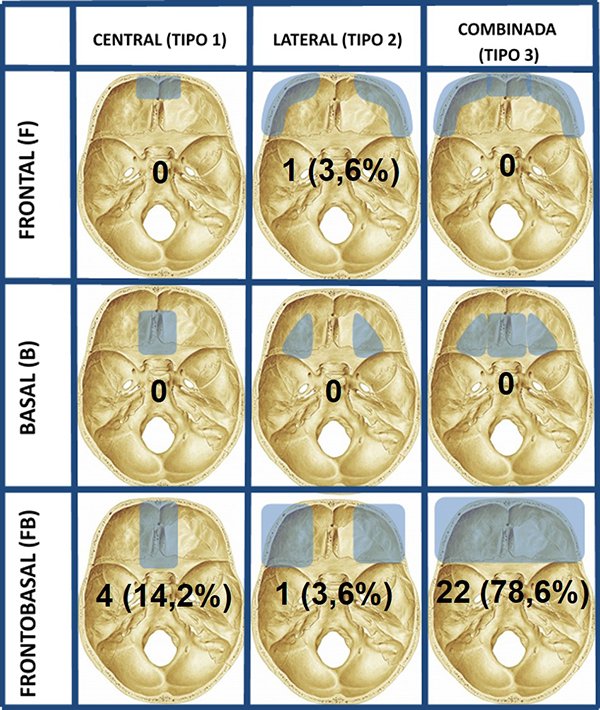
Gráfico 2. Frecuencia según clasificación de las fracturas frontobasales
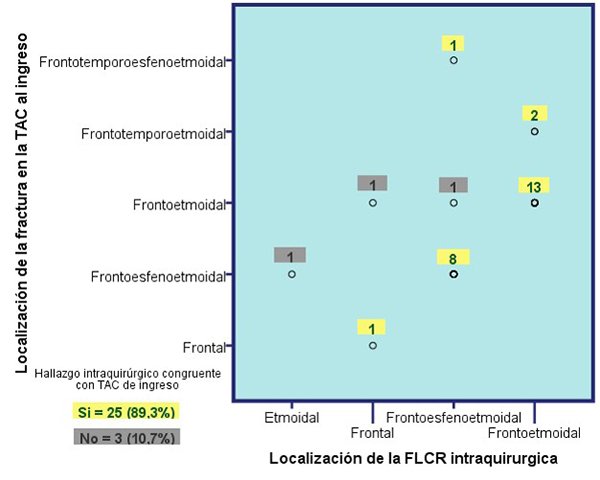
Gráfico 3. Congruencia de localización de FLCR intraquirúrgica con la TAC de ingreso.
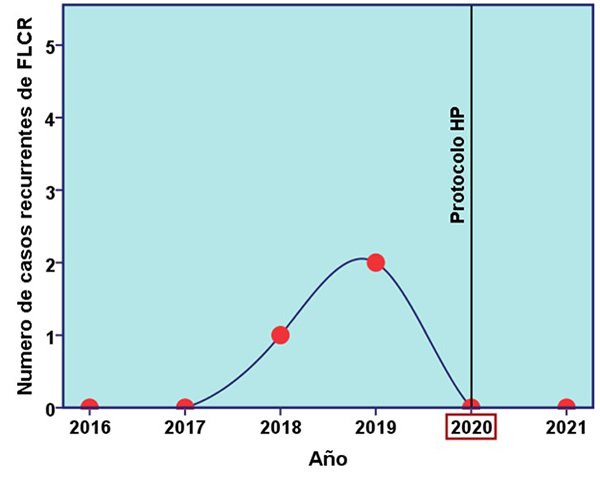
Gráfico 4. Recurrencia de FLCR antes y después de la aplicación del protocolo HP.
DISCUSIÓN
La incidencia de fractura de base de cráneo anterior post traumatismo encéfalo craneano es del 47%, en estos casos hay mayor riesgo de presentar FLCR postraumáticas (33 a 71% frente a 6 a 45% para las fracturas de fosa media),8 ya que el hueso a este nivel es más delgado que el resto de la base del cráneo y existen defectos durales por las perforaciones de los filetes del nervio olfatorio a través de la lámina cribosa del etmoides, haciéndola más propensa a desgarrarse.9
Epidemiología
En este estudio, la mayoría de los pacientes fueron hombres adultos jóvenes y la principal causa del TEC fue accidente en moto sin casco, en estado de embriaguez, igual que en la literatura.1,4,8,9-16
El “engañoso” TEC leve
Es llamativo el alto porcentaje de pacientes con TEC leve y fracturas complejas de base anterior (53,6%). Es un grupo de especial atención, pues su estado neurológico de ingreso es bueno, sin descartar intervenciones quirúrgicas complejas, y es este tipo de TEC el de mayor frecuencia, según la literatura.1,10,13,14
Lesiones asociadas
Todos los pacientes tuvieron lesiones intracraneanas asociadas, en 9 de cada 10 fueron múltiples. Se retrasó la reparación de la FLCR en algunos casos, por la resolución de estas lesiones y estabilización del paciente; 12 (42,9%) pacientes se operaron al ingreso por estas lesiones. En la literatura la presencia de lesiones asociadas va desde 55,8% hasta 74%.1,13,14
Al igual que en este estudio se han reportado en diferentes grados de frecuencia como lesiones asociadas en la literatura: hemorragia subaracnoidea, hematoma extradural, hematoma subdural, edema cerebral, contusiones hemorrágicas, fracturas, neumoencéfalo. La compresión de nervio óptico también se encontró en la literatura, no presentándose en este estudio.1,9,12,15,17
Tiempo desde el TEC hasta el inicio de la FLCR
La mediana del número de días desde que se presentó el TEC hasta el inicio de la FLCR es de 1 día. Un 78,6% fueron fístulas tempranas; de los pacientes con FLCR tardía, un paciente presentó FLCR 16 años después del TEC. Es importante sospechar esta entidad ante la presencia de salida de líquido claro por fosas nasales o deglución de líquido salado, meningitis a repetición en pacientes con antecedentes de TEC. No se debe subestimar este antecedente ni el tiempo que haya trascurrido del mismo. Es importante insistir en los signos de alarma como la rinorraquia en pacientes con fracturas del seno frontal y la base anterior del cráneo que no hayan presentado FLCR o que ésta fue autolimitada con medidas conservadoras; insistir en no confundir estas condiciones con un simple resfriado.
De igual forma la literatura reporta un alto porcentaje de FLCR tempranas, y también un pequeño porcentaje como en este estudio de FLCR tardías, incluso años después (entre 43 a 136 meses), estas últimas se manifestaron mediante meningitis recurrente y rinorraquia tardía.1,9,15,17
Tiempo desde el diagnóstico de la FLCR hasta la cirugía
En este estudio más de la mitad de los pacientes fueron intervenidos quirúrgicamente después de los 7 días desde el TEC, presentándose una mediana de 8,5 días con un rango de 7 a 143 días. Ningún paciente fue intervenido inmediatamente para reparación de la FLCR, debido a la gravedad de sus lesiones y compromiso hemodinámico, requiriendo algunos de éstos, a su ingreso intervención por las lesiones asociadas.
Diferentes autores también han reportado que en más de la mitad de los pacientes realizan la cirugía de reparación de FLCR posterior a los 7 días del TEC, con un rango de días que va de 1 a 180 días desde el TEC, debido a la inestabilidad ya sea por meningitis, edema u otras lesiones de órganos, de igual forma que en este estudio hubo pacientes que requirieron intervenciones inmediatas por otras lesiones craneanas asociadas. (1,12,14,15)
Es discutido en la literatura el momento ideal para la reparación de la FLCR. Por un lado, hay quienes sostienen que realizar la reparación inmediatamente, puede disminuir el riesgo de meningitis y, por otro lado, algunos sugieren esperar al menos una semana post-TEC, para disminuir el edema cerebral y para que la FLCR resuelva espontáneamente.1,9,14,15 Brodie mostró que el riesgo de meningitis es de 8 a 10 veces más elevado si la FLCR dura más de 7 a 10 días.18
Concluimos que la intervención de la reparación de la FCLR se debe realizar lo antes posible en paciente clínicamente estable. Considerando particularmente a aquellos pacientes con marcado edema cerebral o lesiones ocupantes de espacio traumáticas, que aumentan el riesgo de daño del tejido por la retracción. Piek y cols. con respecto al tema, reportó muertes y daño neurológico permanente debido a la retracción del lóbulo frontal.19
Técnica quirúrgica
De acuerdo a la clasificación de Madhusudan a todos los pacientes de este estudio se le realizó un abordaje transcraneal subfrontal. Además, todos ellos posicionados en decúbito supino con cabeza en posición neutra con cabezal de Mayfield, lo que permite un abordaje subfrontal amplio y extenso con alcance límite posterior de la base anterior, permitiendo explorar todas las estructuras que la conforman. El 67,9% requirieron de un abordaje bilateral, el resto unilateral independientemente de rinorraquia uni o bilateral, en base a las características de la fractura en la TC cerebral. Se tuvo en cuenta a aquellos casos en los que la FLCR se manifiesta con rinorraquia unilateral con trazo fracturario en localización contralateral a esta. Acuñamos a esta presentación como FLCR paradojal. Esta situación puede observarse, por ejemplo, en fracturas a nivel del seno esfenoidal cuyos tabiques pueden dirigir la salida del LCR hacia la narina contralateral a la fractura. También puede observarse en pacientes con reparación quirúrgica tardía, rinorraquia unilateral con fracturas bilaterales, en los que un encefalocele impide la salida del LCR de forma bilateral. En estos casos, se hace necesario la exploración bilateral.
En este estudio, ante un defecto óseo importante se rellenó con hueso autólogo (n=10-35,7%-) y/o músculo (n=11-39,3%-) y en 4 (14,3%) pacientes el defecto óseo fue más grande por lo que se usó malla de titanio para evitar el encefalocele. En 22 (78,6%) pacientes se tapizo intraduralmente la fosa anterior con fascia lata y a 8 (28,6%) con pericráneo (dos de estos presentaron recurrencia y requirieron posteriormente recubrir con fascia lata), y en todos se usó cola de fibrina intra y extradural. Por tales recurrencias, desde el 2020, se comenzó a reforzar el tapizado con grasa autóloga intradural en todos los casos.
En la literatura consultada, se objetivó que diversos equipos de referencia realizaron el abordaje transcraneano para las fístulas traumáticas de LCR de base anterior con una técnica quirúrgica equiparable a la utilizada por nuestro equipo.1,9,11,12,14-17,20
Scholsem y cols,1 siempre abordó bilateralmente y utilizó miniplacas y tornillos de titanio para recolocar la plaqueta ósea, limalla ósea y cola de fibrina para rellenar el defecto producto del tratamiento del seno frontal y la lámina cribosa cuando había lesión del nervio olfatorio. Realizó exploración transesfenoidal sublabial microquirúrgica en los pacientes que presentaron recurrencia. Por el contrario, en nuestro trabajo, se realizaron abordajes unilaterales, cuando el lado fracturado en TC cerebral coincidía con el lado de la FLCR y no se usó material de titanio para la recolocación de la plaqueta de rutina. Ésta fue fijada con prolene, ya que muchas de estas fracturas eran abiertas, por ello se trató de emplear la mínima cantidad de material inerte para disminuir el riesgo de infección postquirúrgica. De manera rutinaria, se colocó tejido óseo obturando ambos ostium frontales, completando la acción con un colgajo de músculo temporal pediculado, evitando las fístulas basales. A diferencia de Scholsem y cols. no realizamos reparaciones por vía endoscópica transnasal por el tipo de fracturas.
En todos los casos, nuestra exploración fue intra y extradural, ligándose el seno sagital en la mitad anterior de su tercio anterior debido a la conocida menor incidencia de complicaciones a este nivel. El seno sagital fue ligado en los abordajes bilaterales, que se realizó en el 50% de los pacientes del estudio.
Meco y Oberascher realizaron abordaje transcraneal solo con reparación extradural;20 Friedman y cols. usó otros abordajes como craneotomía con trepano frontal en línea media con exploración extratradural, y algunas veces abordajes combinados (intra y extracraneales).9 Umana y cols. en su metaanálisis muestra que además de la craneotomía frontal también usó abordajes frontonasal y transfrontal sinusal.12 Sheriff y cols. en toda su serie empleó un abordaje bicoronal intradural en la primera cirugía y, en casos de recurrencia realizó un abordaje endoscópico endonasal.14 Rocchi y cols. además del abordaje bicoronal transfrontal, también usó abordaje transfrontal sinusal y frontonasal.15
En el estudio de Zhang y cols. solo realizó apertura dural cuando existía alguna lesión intradural no resuelta,16 a diferencia de nuestra serie.
Se ha propuesto el abordaje extradural en pacientes sin hipertensión intracraneal o con patología intradural, pero los datos de resultados específicos de este enfoque son limitados, hace difícil la identificación del defecto dural y no proporciona control ante complicaciones intradurales, como el hematoma intraoperatorio iatrogénico.14,21
Últimamente, se ha visto un aumento en la reparación mínimamente invasiva de las FLCR por vía endoscópica con buenos resultados, sobre todo en pacientes sin indicación quirúrgica aguda, baja PIC, brechas fistulosas pequeñas y/o tardías a nivel de línea media. Sin embargo, este abordaje es limitado para la reparación de lesiones laterales lejanas, brechas fistulosas mayores a 1 cm y pacientes con factores agravantes como hipertensión intracraneal.
Hallazgo de la brecha fistulosa osteomeningea
Todas las fracturas halladas en este estudio afectaron al hueso frontal y en un 96,4% al etmoides, en menor medida al esfenoides, hallazgos similares a los reportados en la literatura.1,12,14,17,20 Es importante una amplia exploración de la base del cráneo anterior.
Según la clasificación de Madhusudan, en este estudio al igual que en el estudio de Scholsem y cols. y de Zhang y cols,1,16 la mayoría de las fracturas eran FB3, sin hallazgo de fracturas B1, únicas candidatas para resolución endoscópica transnasal transesfenoidal, requiriéndose la reparación transcraneal.
En el estudio de Meco y Oberascher a diferencia nuestra, el porcentaje del compromiso basal del hueso frontal, etmoides y esfenoides fue mayor y el compromiso combinado fue menor, lo que explica que hayan resuelto en mayor proporción la FLCR por vía endoscópica.20
A diferencia de los reportado en la literatura, en el presente estudio se identificaron en el 100% de los casos las laceraciones durales, y en la mayoría de los pacientes la laceración dural y fractura encontrada coincidían con la TC cerebral prequirúrgica.1,12
Los trazos de fractura encontrados en este estudio fueron de mayor tamaño a los reportados en la literatura, siendo mayores a 1 cm, lo que sustenta una vez más la necesidad de la vía transcraneal para la reparación de la FLCR.12,14,22,23
Punción lumbar y uso de DLC
Nuestro protocolo desde el año 2020 establece tomar una muestra de LCR en todos los pacientes para identificar meningitis prequirúrgica. En los estudios reportados en la literatura no se identificó el uso de PL o DLC con este fin, sino con el fin de evacuar LCR ya sea prequirúrgico o postoperatorio para ayudar al cierre de la brecha fistulosa. Tampoco fue usado el DLC con el fin de relajar el cerebro durante la cirugía como en el presente estudio. El tiempo de evacuación del LCR reportado como tratamiento conservador prequirúrgico es de 7 días y post operatorio como adyuvante va 1 a 6 días. La cantidad drenada reportada va de 30 ml a 200 ml día.1,11,12,14-16
Seguimiento, recurrencia
El seguimiento se realizó por mínimo 12 meses y máximo 72 meses. Durante este tiempo en el 89,3% (n=25) de los pacientes requirió una intervención para reparar la FLCR. Solo hubo tres casos (10,7%) de recurrencia de FLCR, uno a los 16 días, a los 83 días y en otro a los 109 días postquirúrgicos. En dos pacientes apareció neumoencéfalo a tensión y uno neumoencéfalo en aumento. Todos requirieron una segunda intervención por vía transcraneana. Los días desde la recurrencia fueron entre 12 ,15 y 143 días, con reparación exitosa tras la segunda cirugía. Desde la implementación del protocolo HP en el 2020 no se reportan recurrencias.
A diferencia de este estudio en la literatura se reporta mayor tiempo de seguimiento desde 2 meses a 384 meses, las recurrencias reportadas fueron variables desde 0% a 14,7%. Fueron reportadas tanto recurrencias tardías como tempranas en el postoperatorio inmediato, las cuales fueren resueltas tanto por vía transcraneal como transesfenoidal, con resolución posterior a la segunda intervención.1,9,12,14-17
El presente estudio tuvo un periodo de seguimiento más corto que la mayoría de las otras series y el tiempo de las recurrencias fue antes del primer año, a diferencia de las otras series.
La recurrencia de FLCR fue mayor en pacientes con Glasgow de 3 en comparación a los de mayor Glasgow, siendo estadísticamente significativo (p=0,02), lo cual podría atribuirse al TEC de alta energía, que provoca mayor lesión ósea y parenquimatosa. La prevalencia de no recurrencia de FLCR fue mayor en aquellos pacientes con FLCR antes de los 7 días desde el TEC, siendo estadísticamente significativo (p=0,015). Los tres pacientes en los que hubo recurrencia presentaron la FLCR después de los 7 días del TEC. No se encontró asociación estadísticamente significativa entre la recurrencia de FLCR y la clasificación de Madhusudan de fracturas de base anterior y tampoco con el porcentaje del área de base anterior ocupado por la fractura. No se reporta este tipo de asociación en la literatura.
Complicaciones
En este estudio, 28,6% pacientes presentaron meningitis. El 25% (7 pacientes) cursaron meningitis prequirúrgica, y 10,7% (3 pacientes) postquirúrgica, cursando dos pacientes con reinfección en el postoperatorio de la FLCR. La literatura reporta entre un 10% a 25% de meningitis en las FLCR por TEC no reparadas, con una mortalidad cercana al 10% (23). La prevalencia en general de meningitis en el contexto de FLCR reportada va desde 18,9 a 27,5%, pre quirúrgica de 5,7 a 17% y postquirúrgica de 1,9 a 16,7%.1,9,12,14,15,17
Se evidencio en este estudio que los pacientes con meningitis tuvieron mayor intervalo desde el diagnóstico a la cirugía con una Me: 13,5 días, que aquellos que no presentaron meningitis (Me 8 días), hallazgo no estadísticamente significativo (p=0,25). A pesar de esto, concuerda con la literatura, en la que se evidencia un aumento del riesgo de meningitis al retrasarse la reparación de la FLCR.9
La prevalencia de meningitis en este estudio fue igual tanto en quienes recibieron o no antibióticos profilácticos, 28,6% en cada grupo (p=0,1). Friedman y cols, tampoco observó diferencias significativas con respecto a esto (10,3% vs 21,4%, respectivamente, p=0,33). Pacientes con FLCR tienen aumentado el riesgo de meningitis y el uso de esta terapia puede tener mayor eficacia en ellos.9 Contrarios a esta postura argumentan que la antibioticoterapia profiláctica es ineficaz en estos pacientes y aumenta la multirresistencia bacteriana. Muchos centros no inician esta terapia a menos que exista una infección clínicamente evidente.14
El germen más frecuentemente identificado en los pacientes con meningitis secundaria a FLCR fue el SAMR (30%), a diferencia del estudio de Friedman y cols. que fue el neumococo.12
También fueron reportados en la literatura algunas complicaciones similares a las de este estudio como abscesos, infección de herida quirúrgica y anosmia. Sin embargo, han sido reportadas otras, como infección de herida quirúrgica, hematoma subdural y extradural, hidrocefalia, hemiparesia y alteración en el estado mental transitorio. Convulsiones y lesiones vasculares no han sido reportadas.1,9,11,12,14-16
La recurrencia de la fístula fue mayor en los que presentaron FLCR después de los siete días desde el TEC, siendo estadísticamente significativo (p=0,015). No hubo asociación estadística entre la presencia de neumoencéfalo y neumoencéfalo a tensión según el porcentaje del área de base anterior ocupado por la fractura. No se encontró este tipo de asociación reportada en la literatura.
Evolución funcional
Durante el tiempo estudiado se presentaron dos óbitos (7,1%): un paciente con secuelas neurológicas con múltiples intercurrencias infecciosas, FLCR persistente, neumoencéfalo a tensión y muerte antes de una tercera intervención (3,6% mortalidad debido a la FLCR); el otro paciente con igual estado neurológico que obitó por neumonía asociada a COVID 19, sin evidencia de recurrencia de FLCR hasta antes del óbito. La mortalidad reportada en la literatura en pacientes con FLCR va de 1,3 a 9,2%.1,13,15,24
El 96,4% de los pacientes presentó curación de la FLCR, valor similar a los de la literatura (90 a 100%).1,14 El 92,9% de los pacientes de este estudio permanece vivos, sin FLCR, 2 (7,1%) pacientes con GOS1 (Glasgow Outcome Score; GOS, Escala de evolución de Glasgow); 1 (3,6%) paciente con GOS3; 2 (7,1%) pacientes con GOS4 y 23 (82,2%) pacientes con GOS5, al igual que en lo reportado en la literatura la mayoría de los pacientes era GOS5.1,4,14
Algoritmo de manejo de FLCR de base anterior
Nuestro algoritmo de trabajo se sintetiza en las Figuras 1 y 2.
A diferencia del algoritmo de Scholsem y cols,1 el nuestro considera el tiempo de evolución de la FLCR, y el estado clínico inicial del paciente para determinar la cirugía. El algoritmo de Sherif y cols. al igual que nosotros, considera la condición clínica al ingreso y los hallazgos en la TC cerebral para determinar el momento de la cirugía. Sin embargo, no considera el tiempo de evolución de la FLCR ni utiliza clasificaciones para orientar el tipo de abordaje a emplear.14
En cuanto al diagnóstico de la FLCR de base anterior es importante resaltar que en la actualidad se cuenta con estudios de imágenes que usan agentes intratecales (fluoresceína, gadolinio, iodados), como lo es la cisternografía por TC, resonancia magnética (RM), cirternografía radioisotópica, útiles cuando la TC multicorte o RM no son diagnósticas; es importante tener en cuenta que los agentes de uso intratecal no son específicos, con excipientes que pueden generar desde una meningitis química, shock anafiláctico o encefalopatía. Por un lado, la fluoresceína de uso oftalmológico que está disponible en nuestro medio no es apta para uso intratecal; el uso de gadolinio intratecal, si bien es el de menor riesgo, no está aún aprobado por la FDA, y se han descrito efectos secundarios como encefalopatía con su utilización; los agentes iodados, si bien están autorizados para uso intratecal, no son inocuos. En este estudio no fue necesario exponer a los pacientes a agentes intratecales debido a que los trazos de fractura y localización de la FLCR fueron evidentes con la TC multicorte de 1 mm.25-28
La reparación de FLCR post-TEC se hace indispensable, ya que la cirugía exitosa reduce desde el 85% al 7% el desarrollo de meningitis a 10 años.1 Por tanto, la preocupación del neurocirujano no debe ser el cese de la rinorraquia, sino la identificación y cierre de la brecha osteomeningea.15
La cirugía está sugerida cuando la FLCR dura más de una semana, cuando se presenta tardíamente, presenta neumoencéfalo o meningocele que perpetua la brecha, cuando el defecto oseo es mayor a 1 cm y el sitio de fuga es múltiple. Se debe procurar la reparación dentro de los primeros 7 días para reducir el riesgo de infección siempre y cuando sea factible.
LIMITACIONES
Este estudio tiene como limitaciones, las propias de los estudios retrospectivos.
Se requieren estudios prospectivos multicéntricos para validar el presente protocolo HP.
CONCLUSIÓN
La aplicación del protocolo HP para fístula nasal traumática de LCR post-TEC tuvo resultados satisfactorios. La tasa de recurrencia fue del 0%.
Los autores no declaran ningún conflicto de interés.
Los autores no declaran financiamiento.
Este es un artículo de acceso abierto bajo la licencia CC BY-NC https://creativecommons.org/licenses/by-nc/4.0/
BIBLIOGRAFÍA