REV ARGENT NEUROC. VOL. 34, N° 2: 92-99 | 2020
ARTÍCULO ORIGINAL
Metástasis sintomáticas en cerebro superiores a 8.5 cm3 manejados con radiocirugía
Eduardo Lovo, Fidel Campos, Víctor Caceros, Mario Minervini, William Reyes
Programa de Radiocirugía Cerebral y Espinal. Centro Internacional de Cáncer, Hospital de Diagnóstico, San Salvador, El Salvador
RESUMEN
Introducción: Las recomendaciones en el manejo de metástasis superiores a 2 cm especialmente las sintomáticas sugieren cirugía como primera opción. En el presente artículo se discute el papel de radiocirugía como primer manejo de estos pacientes.
Material y método: Se evaluaron 37 pacientes sintomáticos con lesiones metastásicas superiores a 8.5 cc tratados con radiocirugía entre el 2011 y el 2018.
Resultados: La media de volumen fue de 12.5 cc (8.5-78.4), 9 (24%) pacientes fueron tratados utilizando LINAC, el volumen medio fue de 20 cc (9.2-70 cc). Los tratamientos con Gamma-Ray fueron administrados a 28 (76%) pacientes, 9 (32%) de ellos en protocolo de radiocirugía adaptativa, la dosis para todo el grupo fue de 13.8 Gy (7.5-18 Gy), con dosis media de 17.9 Gy, el volumen medio fue de 16.3 cc (8.5-78.4 cc) para gamma. El Karnofsky al inicio era de 60 (50-70) y de 80 (60-100) a los 30 días (P=0.0001). A los 30 días, 95% de las lesiones habían reducido su tamaño en un 74% (11-95%). La sobrevida media de la serie fue de 19 meses (4-34), el riesgo acumulado de muerte del SNC fue de 5.4%.
Conclusiones: Radiocirugía en nuestra experiencia ha mostrado ser eficaz en el control de metástasis a cerebro de gran tamaño, reduciendo la necesidad de cirugía.
Palabras Clave: Cerebro; Metástasis; Cáncer de Mama; Radiocirugía; Neurocirugía; GammaKnife; Aceleradores Lineales
ABSTRACT
Introduction: Current recommendations with regards to metastases larger than 2 cm specially in symptomatic patients suggest surgery as a first choice. We analyze the role of upfront radiosurgery as first line of treatment in such patients.
Methods: 37 symptomatic patients that harbored tumors greater than 8.5 cc in volume were treated from 2011 to January 2018.
Results: The median tumor volume was 12.5 cc (8.5-78.4), 9 (24%) patients were treated with LINAC with a volume of 20 cc (9.2-70 cc). The treatments with GammaRay were administrated to 28 (76%) patients, 9 (32%) of them with adaptive radiosurgery protocol, the prescription dose for the gamma group was 13.8 Gy (7.5-18Gy) mean dose of 17.9 Gy (13.2-23.3 Gy) with a mean volume of 16.3 cc (8.5-78.4 cc). Karnofsky score was 60 (50-70) the day of treatment and 80 (60-100) at 30 days (P=0.0001). At 30 days, 95% of the tumors had reduced in size in a 74% (11-95%) for those evaluated. Median survival was 19 months (4-34), with an accumulative risk of death from central nervous progression of 5.4%.
Conclusions: Radiosurgery in our experience has shown to be effective in controlling large metastases, reducing the need for open surgery.
Key words: Brain; Metastases; Breast Cancer; Radiosurgery; Neurosurgery; Gamma Knife; Linear Accelerators
Los autores declaran no tener ningún conflicto de interés.
Eduardo Lovo
lovoiglesias@gmail.com
Recibido: Diciembre de 2019. Aceptado: Marzo de 2020.
INTRODUCCIÓN
Las metástasis a cerebro son los tumores más comunes del sistema nervioso central, la incidencia es desconocida en Latinoamérica y es posible que varíe en relación con las posibilidades de sobrevida al diagnóstico inicial de cáncer. Sabemos que la sobrevida es diferente entre países desarrollados y subdesarrollados,4 aumentando la incidencia de metástasis a aquellos pacientes que sobreviven más tiempo, especialmente en el cáncer de mama. Las metástasis al cerebro representan una causa frecuente de consulta en los servicios de radioterapia y en neurocirugía, por lo cual tener criterios claros de selección para cirugía tiene importancia.
Las guías más recientes en el 2019 (V1) de la National Comprehensive Cancer Network (NCCN) y las del Congress of Neurological Surgeons (CNS) recomiendan cirugía en el manejo de metástasis a cerebro en número limitado de lesiones, definidas entre 1 a 3 tumores con historia conocida de cáncer, como primera opción en caso de síntomas y efecto de masa. En cuanto a la toma de decisiones, estas guías sugieren que lesiones superiores a 2 cm pueden ser mejor manejadas por vía de cirugía.5,18
El manejo radioquirúrgico de lesiones tumorales de origen metastásico de “gran tamaño” representan un dilema para esquemas de fracción única y radiocirugía fraccionada en cuanto a una dosis de radiación segura que limite la toxicidad en el tejido cerebral adyacente y que a su vez sea efectiva en el control tumoral a largo plazo.6,8,30 Existe correlación de dosis y control a largo plazo que demuestran que, a menor dosis menor control. Usualmente a mayor tamaño de lesión menor dosis de radiación se administra según las recomendaciones de la RTOG 90-05.24 No obstante, la práctica y la literatura muestran que lesiones grandes también pueden ser manejadas utilizando radiocirugía, existe evidencia de control tumoral a largo plazo,12,26,31 y variantes en la técnica conocidas como radiocirugía en dos tiempos o adaptativa que comienzan a presentar resultados que hacen factible tratar tumores grandes con radiocirugía.2,7,9,10,13,15,16 Recientemente, nuestro grupo publicó el primer artículo en donde se plantea la radiocirugía en dos sesiones como una alternativa a cirugía en el tratamiento de tumores grandes de histología conocida de mama y pulmón, en pacientes que experimentaban síntomas neurológicos.15
La presente serie muestra la evolución en tratamientos y la experiencia ganada utilizando diferentes esquemas radioquirúrgicos en el manejo de enfermedad metastásica cerebral en lesiones superiores a 8.5 centímetros cúbicos (CC) en volumen o lo que equivale como mínimo a una esfera de 2.5 cm de diámetro en pacientes con síntomas neurológicos.
MATERIAL Y MÉTODOS
De manera retrospectiva se evaluó 37 pacientes que acudieron a consulta y tratamiento estando sintomáticos con lesiones metastásicas a cerebro cuyo volumen era superiores a 8.5 cc, los pacientes fueron tratados con radiocirugía en el Centro Internacional de Cáncer desde febrero del 2011 hasta enero del 2018. Durante este periodo se utilizó un LINAC conocido como Tomoterapia™ (Accuray, Sunnyvale, California. USA) bajo esquemas de irradiación en dosis únicas o radiocirugía fraccionada, y a partir del 2014 radiocirugía en sesión única o en radiocirugía de dos sesiones utilizando el bisturí de rayos gamma rotatorio Infini™ (Masep® Technology Industries. Shenzhen, China). En 12 pacientes se realizó resonancia magnética antes de los 30 días ya sea como parte de los protocolos de radiocirugía (neoadyuvante) preoperatoria de la institución, radiocirugía en dos sesiones o para evaluar velocidad de respuesta en cuanto a la reducción del tamaño tumoral se refiere.
Todos los pacientes padecían de dolor de cabeza, náuseas y/o vómitos, hemiparesia en grados diversos, alteración del habla, alteraciones visuales, síntomas demenciales, hidrocefalia o una mezcla de síntomas atribuibles al efecto de masa producido por el o los tumores. Todos los pacientes recibieron una consulta neuroquirúrgica previa al tratamiento con radiocirugía, a los pacientes y sus familiares se les explicó que según las normas vigentes el manejo del tumor ameritaba manejo quirúrgico, que se practicaría radiocirugía y que en caso de existir deterioro neurológico en los siguientes días se realizaría cirugía abierta con la posible ventaja que según las investigaciones sobre radiocirugía neoadyuvante (antes de cirugía) mostraban tendencia a reducir la posibilidad de diseminación leptomeníngea (ver discusión). Habiendo resuelto dudas, los pacientes y sus familiares firmaban el consentimiento informado.
En el día de la simulación para LINAC o del tratamiento para Infini™, todos los pacientes recibieron una dosis de dexametasona de 8 mg endovenosa como parte de su preparación, la resonancia magnética de ese día fue hecha con una Resonador Avanto™ (Siemens. Erlangen, Alemania) de 1.5 tesla, utilizando una doble dosis de gadolinio (Gadovist) y retrasando la adquisición de imágenes de T1-Gadolinio axiales de 1mm de espesor de todo el encéfalo entre 10 a 15 minutos. Para el LINAC se utilizó un marco no invasivo conocido como PinPoint™ (Aktina Medical, Congers, NY, USA) y en el caso de Infini™ un marco estereotáctico invasivo estándar, colocándolo bajo sedación ligera y anestesia local. Imágenes fueron enviadas a MIMVista (MIM Software Inc. Cleveland, OH, USA) en caso del LINAC y para Superplan (Masep® Technology Industries. Shenzhen, China) en el caso de Infini™. Neurocirugía y Radioterapia fueron los responsables de contornear las lesiones para generar los PTV (Planned Target Volume) respectivos y los OR (Órganos en Riesgo). Las dosis fueron ajustadas según máquinas, cantidad de lesiones o tratamientos previos o posteriores.
La mayoría de los casos fueron dados de alta de manera inmediata, a los pacientes se les controlaba por teléfono a las 24 horas y 72 horas para corroborar que no existiera empeoramiento de sus síntomas neurológicos y usualmente con indicación de tomar dexametasona 2 mg cada 8 horas hasta su próximo control con neurocirugía usualmente en siete a 10 días. En el caso de los pacientes tratados con radiocirugía de dos sesiones con Infini™, los pacientes regresaban a los 30 días para un segundo tratamiento en el cual básicamente se repetían los pasos específicos para Infini™ ya descritos y se entregaba un nuevo tratamiento “adaptando” el PTV al nuevo volumen de la lesión y fraccionando las dosis de manera equitativa en la mayoría de los casos entre la primera y segunda sesión. Las dosis más habituales utilizadas procuraban una dosis media de 15 Gy y 15 Gy como mínimo en cada tratamiento.
Los pacientes fueron evaluados en los meses siguientes y seguimiento continuo por vía telefónica o presencial hasta que fallecían o hasta finalizar el presente estudio.
RESULTADOS
La edad media de los pacientes fue de 59.5 años (37-79), la mayoría de los pacientes eran mujeres cuya enfermedad primaria era cáncer de mama 89% (33), los otros pacientes masculinos padecían cáncer de pulmón (2), cáncer de mandíbula (1) y linfoma gástrico en un caso. La media de volumen por lesión fue de 12.5 cc (8.5-78.4), la media de cantidad de lesiones por paciente fue de 3 (1-8), un total de 111 tumores fueron tratados con radiocirugía en estos pacientes de los cuales 42 tumores superaban los 8.5 cc como volumen individual por tumor en los 37 pacientes estudiados. Nueve (24%) pacientes fueron tratados utilizando Tomoterapia bajo esquemas diversos de dosis y fraccionamientos, 2 pacientes recibieron fracciones en dosis única de 12 Gy, 5 de ellos recibieron 3 fracciones de 7 Gy y el resto 5 fracciones de 5 Gy, el volumen medio de los tumores tratados con tomoterapia fue de 20cc (9.2-70 cc).
Los tratamientos con Infini™ fueron administrados a 28 (76%) pacientes, 19 (67%) de ellos en una sola fracción y 9 (32%) de ellos en protocolo de radiocirugía adaptativa, la dosis de prescripción para todo el grupo fue de 13.8 Gy (7.5-18Gy) a la curva del 50%, con dosis media en el PTV de 17.9 Gy (13.2-23.3Gy), con un volumen medio de 16.3 cc (8.5-78.4 cc). Para el protocolo de radiocirugía de dos sesiones la dosis de prescripción fue de 14.5 Gy (10-18) con una dosis media de 20.5 Gy (13.2-23-3) en la primera sesión a un volumen de 12.8 cc (8.5-78.4) y de 13.5 Gy (10-18) con una dosis media de 18.6 Gy (13-26) en la segunda sesión a los 30 días a un volumen de 4.3 cc (0.4-70) por efecto del tratamiento inicial y la consecuente reducción del tamaño tumoral (figs. 1 y 2).
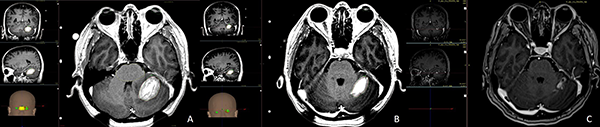
Figura 1: A) Muestra una lesión metastásica de cáncer de mama en cerebelo izquierdo de 11.2 cc en volumen y se administraron 12 Gy como dosis marginal a la curva isodosica del 50% (Dosis media de 16.6 Gy). B) Segunda sesión a los 30 días en donde la lesión ha reducido su volumen a 4.9 cc representando una reducción del 56%, el efecto de masa sobre el cuarto ventrículo ha sido resuelto, se prescribió una nueva dosis de radiocirugía ahora con 15 Gy como dosis marginal a la curva isodósica del 50% (Dosis media de 19.7 Gy). C) A los tres meses la lesión mide 1.3 cc.
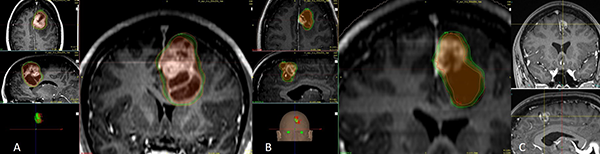
Figura 2: A) Metástasis frontal izquierda de cáncer de mama con receptores hormonales negativos que produce efecto de masa midiendo en la primera sesión de radiocirugía 37 cc en su volumen inicial, la dosis de prescripción es 12 Gy a la curva del 50% señalizada en verde, la sombra anaranjada representa todo el volumen interno que está recibiendo más de 15 Gy. B) Imágenes durante el segundo tratamiento a los 30 días, el volumen de la lesión se ha reducido 62% (vol. 14cc) la nueva dosis de prescripción es 12 Gy a la curva del 50% señalizada en verde, la sombra anaranjada representa todo el volumen interno que está recibiendo más de 15 Gy. C) Control a los 3 meses, el efecto de masa ha sido resuelto por completo.
Todos los pacientes se encontraban sintomáticos al inicio del tratamiento, su nota media de Karnofsky (KPS) debido a sus síntomas neurológicos al inicio fue de 60 (50-70) y de 80 (60-100) a los 30 días (P=0.0001).
En 21 (50%) tumores superiores a 8.5 cc en 12 pacientes se pudo hacer RM antes de o a los 30 días, 95% (20) de las lesiones habían reducido su tamaño en una media de 74% (11-95%) con un volumen inicial medio de 12.8 cc y de 4.3 cc al control, solo 1 lesión quística incremento su tamaño un 53% y necesito manejo quirúrgico a los 4 meses posterior al tratamiento.
Hubo reportes de 7 (18.9%) pacientes que desarrollaron radionecrosis o progresión manifestado por crecimiento en por lo menos 1 de las lesiones irradiadas según RECIST (Response Evaluation Criteria in Solid Tumors), dos de ellos fueron manejados con éxito con medidas anti-edema y vitamina E. De la totalidad de la serie 6 (16.2%) pacientes fueron re-irradiados utilizando radiocirugía y 2 pacientes de la serie fallecieron por progresión de su enfermedad a nivel cerebral a los 7 y 34 meses. Ningún paciente de la serie requirió de cirugía antes de los 3 meses posteriores a radiocirugía. No hubo diferencia estadísticamente significativa en sobrevida en los pacientes que recibieron dosis única con Tomoterapia o Infini versus aquellos que recibieron dos sesiones (17.9 versus 22.8 meses respectivamente) P=0.29.
Al final del estudio cuatro pacientes incluyendo los dos que fallecieron reunían criterios de necesitar cirugía para aliviar efecto de masa por crecimiento de la lesión o radionecrosis posterior a radiocirugía, el tiempo promedio para requerir cirugía fue a los 7 meses (4-34) después del tratamiento, tres de ellos tuvieron acceso a cirugía incluyendo la paciente que presento crecimiento de la lesión quística la cual fue operada al 4to mes posterior a la radiocirugía. La paciente que falleció por progresión antes del año no tuvo acceso a cirugía. No hubo reportes de diseminación leptomeníngea posterior a radiocirugía.
La sobrevida media de la serie fue de 19 meses (4-34), la sobrevida al año fue del 60% de la serie (graf. 1) con un riesgo acumulativo de muerte por progresión local o a distancia en el sistema nervioso central (SNC) del 5.4%. El resto de los pacientes fallecieron por progresión de su enfermedad primaria.

Gráfico 1: Curva de sobrevida, la sobrevida media global fue de 19.6 meses. La probabilidad de sobrevivir al año fue del 60% y del 32% a los 2 años.
DISCUSIÓN
Existen dificultades que incluyen control tumoral y progresión al igual que riesgos inherentes al manejo de metástasis de gran tamaño en cerebro. Para la cirugía un riesgo importante es el de diseminación leptomeníngea (DLM) el cual puede oscilar entre el 13% al 50%, especialmente en fosa posterior y cuando la lesión no es removida en bloque,1,27-29 a mayor tamaño de la lesión es técnicamente más complejo removerlas “en bloque” sin el riesgo de ocasionar déficit neurológico. Nuestro grupo recientemente público su experiencia en más de 200 craneotomías con el paciente despierto y resección de tumores intrínsecos que incluyen metástasis, como era de esperar a mayor cercanía de la lesión en relación con áreas elocuentes mayor posibilidad de ocasionar alteraciones neurológicas y de una resección incompleta.14 El resecar parcialmente una metástasis no es un tema menor, se asocia a menor sobrevida,17,20 por lo cual el máximo cuidado debe de ser tomado para remover por completo las metástasis en caso de que la cirugía sea efectuada. Debido a los riesgos de diseminación intrínsecos a la cirugía han surgido protocolos de radiocirugía neo adyuvancia (previa) a cirugía que han demostrado en algunas series eliminar o reducir el riesgo de DLM y de radionecrosis sintomática,26-28 a pesar de que los resultados aún no son concluyentes, la radiocirugía previa (neoadyuvante) en oposición a radiocirugía después de la cirugía parece tener algunas ventajas.3 Existen otros riesgos inherentes de la cirugía cerebral que no pueden ser obviados como déficit neurológico, infección, fístulas o dehiscencia y dependerán de la experiencia quirúrgica de cada centro y las condiciones generales del paciente. Aunque este tema escapa de la presente discusión, también es de hacer notar que la cirugía clásicamente se reserva para pacientes con lesiones únicas y para pacientes con buen estado de KPS lo cual no es lo más común de ver en pacientes sintomáticos por metástasis cerebrales.
En los años que se llevó acabo el presente estudio, nuestro grupo ofrecía radiocirugía antes de cirugía para lesiones voluminosas con efecto de masa y que producían síntomas, sin embargo en estos pacientes se notaba mejoría clínica a veces tan rápido como las 24 horas posterior a la irradiación del tumor, cuando la cirugía por alguna razón se retrasaba más allá de 72 horas, se comenzó a ver reducción del volumen tumoral en la Resonancia Magnética adquirida el día de la cirugía para navegación (Cirugía Guiada por Imágenes). Producto de este acúmulo de casos de radiocirugía antes de cirugía y las mejorías que notábamos posteriormente a la irradiación del tumor se decidió dejar la opción quirúrgica como la última elección solo en caso de que radiocirugía fallase en revertir u ocasionara empeoramiento de los síntomas neurológicos en los pacientes. Una de las debilidades del presente estudio es su variabilidad en cuanto a máquinas y esquemas radioquirúrgicos, sin embargo, cabe mencionar que no era el objetivo demostrar superioridad de una técnica radioquirúrgica sobre otra, sino de la efectividad de radiocirugía en general para reducir la necesidad de operar a pesar de las recomendaciones actuales sobre efecto de masa y el tamaño de las lesiones en pacientes sintomáticos. La mejoría clínica según KPS a los 30 días fue notoria y estadísticamente significativa. Ningún paciente de la serie necesitó cirugía antes de los tres meses por empeoramiento de los síntomas lo cual deja entrever que radiocirugía como tratamiento inicial en lesiones metastásicas superiores a 2.5 cm de diámetro es un tratamiento seguro y efectivo, el cual evita la cirugía la mayoría de las veces.15
La sobrevida acá reportada es comparable con las series más optimistas de metástasis cerebrales provenientes de cáncer de mama,11,19 desconocemos por qué nuestro centro recibe un porcentaje tan alto de metástasis de mama en comparación a las otras histologías, pero sospechamos que tiene que ver con la sobrevida en base a manejo del cáncer primario en países en vías de desarrollo como en el que se realizó la presente investigación. Solo una paciente falleció por aumento del tamaño de una de las lesiones metastásicas en cerebro antes del año y la razón fue porque no tuvo acceso a cirugía. Cabe mencionar que esta paciente es de la serie de radiocirugía adaptativa y que el aumento de la lesión en su último control correspondía por aspecto radiológico a radionecrosis. Esta paciente en conjunto con los otros cuatro que si fueron intervenidas quirúrgicamente solidifican el verdadero “Matrimonio” que debe existir entre radioterapia y neurocirugía. El hecho de que ocurra radionecrosis o exista progresión tumoral que eventualmente puedan requerir cirugía no refleja un “fracaso” de la técnica radioquirúrgica, ejemplifica la complejidad en el manejo de estas lesiones. Esta serie deja entrever lo que podemos lograr hoy en día en beneficio de la calidad de vida de los pacientes oncológicos metastásicos al favorecer tratamientos no invasivos y el acceso a neurocirugía cuando sea necesario.
La presente serie demuestra que el manejo no quirúrgico por vía de radiocirugía en lesiones superiores de 2.5 cm es viable, y que el alivio de los síntomas neurológicos es rápido debido al efecto marcado en reducción del volumen tumoral que la radiocirugía ofrece. A lo largo de los siete años de funcionamiento de la unidad de radiocirugía cráneo espinal en nuestro centro el manejo y toma de decisiones en cuanto a este tipo de lesiones ha cambiado en base a la evidencia que este artículo reporta.
Finalmente, como grupo neuroquirúrgico con práctica neurooncológica de más de una década podemos afirmar que la radiocirugía ha modificado nuestro abordaje de metástasis cerebrales de gran tamaño, en la práctica nos cuesta cada vez más poder determinar una recomendación estándar sobre síntomas neurológicos. No hemos tenido un caso extremo en donde los síntomas ameritaron una intervención neuroquirúrgica de emergencia por metástasis a cerebro sin que tuviéramos oportunidad de estabilizar y poder dar radiocirugía primero.
Nuestra unidad posee capacidades que reconocemos no están ampliamente disponibles en la mayoría de los centros en América Latina. En primer lugar, tenemos una población relativamente cautiva de pacientes conocidos por cáncer, también somos una institución privada lo cual puede influir en las emergencias neuroquirúrgicas que recibimos. En segundo lugar, nuestros pacientes tienen acceso a radiocirugía con la misma velocidad o en ocasiones más rápido que a una cirugía abierta con costos monetarios en radiocirugía que suelen ser la mitad de los costos relacionados a una cirugía. La inmediata disponibilidad a radiocirugía podría influir en la mayoría de los resultados que esta investigación demuestra.
CONCLUSIONES
Radiocirugía en nuestra experiencia ha mostrado ser eficaz en el control de metástasis a cerebro de gran tamaño, la seguridad y toxicidad reportada está dentro de lo esperado en lesiones más pequeñas.
La combinación de radiocirugía temprana y manejo de esteroides revierte los síntomas producto de efecto de masas en la mayoría de los pacientes, reduciendo la necesidad de cirugía. Es importante recalcar el involucramiento neuroquirúrgico durante el tratamiento de radiocirugía, Nuevos esquemas de tratamiento radioquirúrgicos en combinación con cirugía cuando se pierde el control tumoral o existe radionecrosis son necesarios para procurar la máxima efectividad con la menor alteración de calidad de vida en pacientes con cáncer.
BIBLIOGRAFÍA
- Ahn JH, Lee SH, Kim S, Joo J, Yoo H, Lee SH, et al. Risk for leptomeningeal seeding after resection for brain metastases: implication of tumor location with mode of resection. J Neurosurg. 2012;116:984-93.
- Angelov L, Mohammadi AM, Bennett EE, Abbassy M, Elson P, Chao ST, et al. Impact of 2-staged stereotactic radiosurgery for treatment of brain metastases ≥ 2 cm. J Neurosurg. 2017;22:1-17.
- Asher AL, Burri SH, Wiggins WF, Kelly RP, Boltes MO, Mehrlich M, et al. A new treatment paradigm: neoadjuvant radiosurgery before surgical resection of brain metastases with analysis of local tumor recurrence. Int J Radiat Oncol Biol Phys. 2014;88:899-906.
- Bernard W. Stewart and Christopher P. Wild. World cancer report 2014, International Agency for Research on Cancer. World Health Organization Press. http://www.who.int/cancer/publications/WRC_2014/en/
- Clinical Practice Guidelines in Oncology. Central Nervous System Cancers, Limited Brain Metastases. Version 1.2019 https://www.nccn.org/professionals/physician_gls/default.aspx#cns
- De Azevedo Santos TR, Tundisi CF, Ramos H, Maia MA, Pellizzon AC, Silva ML, et al. Local control after radiosurgery for brain metastases: predictive factors and implications for clinical decision. Radiat Oncol. 2015;10:63.
- Dohm A, McTyre ER, Okoukoni C, Henson A, Cramer CK, LeCompte MC, et al. Staged Stereotactic Radiosurgery for Large Brain Metastases: Local Control and Clinical Outcomes of a One-Two Punch Technique. Neurosurgery. 2018;81: 114-121
- Ebner D, Rava P, Gorovets D, Cielo D, Hepel JT. Stereotactic radiosurgery for large brain metastases. J Clin Neurosci. 2015;22:1650-4.
- Frischer JM, Fraller A, Mallouhi A, Vogl UM, Baier F, Ertl A, et al. Evaluation of Dose-Staged Gamma Knife Radiosurgical Treatment Method for High-Risk Brain Metastases. World Neurosurg. 2016;94:352-9.
- Hasegawa T, Kato T, Yamamoto T, Iizuka H, Nishikawa T, et al. Multisession gamma knife surgery for large brain metastases. J Neurooncol. 2017;131:517-524.
- Jaboin JJ, Ferraro DJ, DeWees TA, Rich KM, Chicoine MR, Dowling JL, et al. Survival following gamma knife radiosurgery for brain metastasis from breast cancer. Radiat Oncol. 2013;8:131.
- Jeong WJ, Park JH, Lee EJ, Kim JH, Kim CJ, Cho YH. Efficacy and Safety of Fractionated Stereotactic Radiosurgery for Large Brain Metastases. J Korean Neurosurg Soc. 2015;58:217-24.
- Kim JW, Park HR, Lee JM, Kim JW, Chung HT, Kim DG, et al. Fractionated Stereotactic Gamma Knife Radiosurgery for Large Brain Metastases: A Retrospective, Single Center Study. PLoS One. 2016;11:e0163304.
- Lovo E, Minervini M, Ahues E, Martinez-Cortez R, Milla R, Cruz C: Safety and tolerability of awake craniotomy for brain tumors and other supratentorial lesions. Rev Argent Neuroc. 2018;32:258-264.
- Lovo EE, Torres LB, Campos FJ, Caceros VE, Barahona KE, Minervini MH, Reyes WA. Two-session Radiosurgery as Initial Treatment for Newly Diagnosed Large, Symptomatic Brain
- Metastases from Breast and Lung Histology. Cureus. 2019;24:e5472.
McTyre E, Helis CA, Farris M, Wilkins L, Sloan D, Hinson WH, et al. Emerging Indications for Fractionated Gamma Knife Radiosurgery. Neurosurgery. 2017;80:210-6.
- Munoz-Bendix C, Rapp M, Mijderwijk HJ, et al.: Risk factors for in-brain local progression in elderly patients after resection of cerebral metastases. Sci Rep. 2019;15:7431.
- Nahed BV, Alvarez-Breckenridge C, Brastianos PK, Shih H, Sloan A, Ammirati M et al.: Congress of Neurological Surgeons systematic review and evidence-based guidelines on the role of surgery in the management of adults with metastatic brain tumors. Neurosurgery. 2019;84:E152-5.
- Patel KR, Burri SH, Boselli D, Symanowski JT, Asher AL, Sumrall A, et al.: Comparing preoperative with postoperative stereotactic radiosurgery for resectable brain metastases: a multi-institutional analysis. Neurosurgery. 2016, 79:279-85.
- Patel AJ, Suki D, Hatiboglu MA, Rao VY, Fox BD, Sawaya R. Impact of surgical methodology on the complication rate and functional outcome of patients with a single brain metastasis. J Neurosurg. 2015;122:1132-43. doi: 10.3171/2014.9.JNS13939
- Prabhu RS, Patel KR, Press RH, Soltys SG, Brown PD, Mehta MP, et al. Preoperative Vs Postoperative Radiosurgery for Resected Brain Metastases: A Review. Neurosurgery. 2018;16: 19-29.
- Rades D, Dziggel L, Janssen S, Blanck O, Hornung D, Schild SE. A Survival Score for Patients Receiving Stereotactic Radiosurgery Alone for Brain Metastases from Breast Cancer. Anticancer Res. 2016;36:1073-6.
- Shaw E, Scott C, Souhami L, Dinapoli R, Kline R, Loeffler, et al. Single dose radiosurgical treatment of recurrent previously irradiated primary brain tumors and brain metastses: Final report of RTOG protocol 90-05. Int. J. Radiat. Oncol. Biol. Phys. 2000;47:291–298.
- Siomin VE, Vogelbaum MA, Kanner AA, Lee SY, Suh JH, Barnett GH. Posterior fossa metastases: risk of leptomeningeal disease when treated with stereotactic radiosurgery compared to surgery. J Neurooncol. 2004;67:115-21.
- Soliman H, Das S, Larson DA, Sahgal A. Stereotactic radiosurgery (SRS) in the modern management of patients with brain metastases. Oncotarget. 2016;15:12318-30.
- Suki D, Abouassi H, Patel AJ, Sawaya R, Weinberg JS, Groves MD. Comparative risk of leptomeningeal disease after resection or stereotactic radiosurgery for solid tumor metastasis to the posterior fossa. J Neurosurg. 2008;108:248-57.
- Suki D, Hatiboglu MA, Patel AJ, Weinberg JS, Groves MD, Mahajan A, et al. Comparative risk of leptomeningeal dissemination of cancer after surgery or stereotactic radiosurgery for a single supratentorial solid tumor metastasis. Neurosurgery. 2009;64:664-74.
- Van der Ree TC, Dippel DW, Avezaat CJ, Sillevis Smitt PA, Vecht CJ, van den Bent MJ. Leptomeningeal metastasis after surgical resection of brain metastases. J Neurol Neurosurg Psychiatry. 1999;66:225-7
- Vogelbaum MA, Angelov L, Lee SY, Li L, Barnett GH, Suh JH. Local control of brain metastases by stereotactic radiosurgery in relation to dose to the tumor margin. J Neurosurg. 2006;104:907-911.
- Wegner RE, Leeman JE, Kabolizadeh P, Rwigema JC, Mintz AH, Burton SA, et al. Fractionated stereotactic radiosurgery for large brain metastases. Am J Clin Oncol. 2015;38:135-9.
COMENTARIO
Los autores reportan su experiencia en el tratamiento de metástasis mayores de 20 mm de diámetro, sintomáticas e incluso únicas del SNC con radiocirugía. Si bien tienen en su serie un grupo heterogéneo de pacientes en quienes se utilizó rayos X, rayos Gamma, sesión única, dos sesiones o terapia fraccionada, los resultados globales reflejan buena respuesta en los controles iniciales con reducción del tamaño tumoral a los 30 y 90 días. Aunque es una estrategia que los autores consideran de primera línea en su lugar de trabajo, el lector joven debe recordar que en líneas generales la indicación respecto a una metástasis única, sintomática y superior de 10 mm es quirúrgica. Los riesgos de diseminación leptomeníngea disminuyen notablemente con el uso de una entrenada técnica microquirúrgica de resección en bloque sin el uso de aparatos de cavitación ultrasónica, que han sido descriptos como predisponentes de dejar residuos de lesión no visualizables al terminar la cirugía, que aumentan el riesgo de recidiva y diseminación. Una manera de evaluar la verdadera superioridad o no del tratamiento radiante es compararlo con un grupo que hubiese optado por cirugía e incluir un seguimiento más prolongado de los casos. Por último, si bien es complejo el acceso a este tipo de terapia en los países en vías de desarrollo, no hay dudas que la radiocirugía es la alternativa en lesiones de áreas no resecables (pedúnculo cerebeloso, tronco cerebral, ganglios de la base), menores de 10 mm, múltiples o con un “status performance” oncológico adverso.
Tomás Funes
Sanatorio Anchorena. C.A.B.A., Argentina
COMENTARIO
Los autores evalúan el tratamiento con radiocirugía en pacientes sintomáticos con lesiones metastásicas superiores a 8.5 cc. Históricamente las metástasis de gran volumen, mayores de 3 cm han tenido indicación de microcirugía.1
Estos trabajos, en donde se evalúa el tratamiento en lesiones previamente consideradas para cirugía, vienen a poner luz sobre el potencial alcance de la radiocirugía para el tratamiento de las metástasis cerebrales, y conocer cual es el limite de tamaño en el tratamiento con radiocirugía.2
Me parece que este estudio resulta muy útil, en especial para pacientes que no son candidatos para cirugía por alguna razón, ya sea localización en área elocuente de la lesión o incapacidad del paciente de tolerar una cirugía, o en aquellos con una sobrevida muy corta por su enfermedad de base.
Pablo Ajler
Hospital Italiano de Buenos Aires. C.A.B.A., Argentina
BIBLIOGRAFÍA
- Andrews DW, Scott CB, Sperduto PW, Flanders AE, Gaspar LE, Schell MC, et al: Whole brain radiation therapy with or without stereotactic radiosurgery boost for patients with one to three brain metastases: phase III results of the RTOG 9508 randomised trial. Lancet 363:1665–1672, 2004.
- Lee CC, Yen CP, Xu Z, Schlesinger D, Sheehan J. Large intracranial metastatic tumors treated by Gamma Knife surgery: outcomes and prognostic factors. J Neurosurg. 2014;120(1):52–59.
COMENTARIO
Los autores realizaron un estudio retrospectivo, con una n pequeña para 7 años de pacientes tratados con radiocirugía, para lo cual se utilizó dos aparatos de entrega de dosis radiante y protocolos dispares. No mencionan los otros tratamientos que los pacientes pudieron recibir durante el período de seguimiento (quimioterapia, monoclonales, terapias blanco). Tampoco las escalas de calidad de vida aplicadas. Demás está decir que la sola administración de corticosteroides produce respuestas espectaculares en algunos de estos pacientes dentro de las 24 hs; por ende, atribuir esta mejoría al tratamiento radiante es, al menos, algo aventurado. Asimismo, los autores hacen notar que “la cirugía clásicamente se reserva para pacientes con lesiones únicas y para pacientes con buen estado de KPS lo cual no es lo más común de ver en pacientes sintomáticos por metástasis cerebrales”. No puedo estar menos que en desacuerdo, ya que un paciente con metástasis en fosa posterior puede tener un Karnofsky muy bajo, pero con enfermedad controlada; y el mismo, una vez evacuada la lesión que provocaba efecto de masa en el tronco encefálico y/o hidrocefalia no comunicante, podrá tener una evolución favorable, sólo para dar un ejemplo. La “mano” y “criterio” de resección del neurocirujano siempre será fundamental para el mejor gesto quirúrgico llevado en el paciente.
En este trabajo, los autores incluyeron en su casuística retrospectiva un 89% con cáncer de mama. Es bien sabido que el tipo de tumor primario influye en la supervivencia media, con rangos que incluyen 2.7 a 6.3 meses para pulmón, 5.1 a 6 meses para colorrectal y 4.8 a 10 meses para el melanoma. Además, la supervivencia para el cáncer de mama difiere según los subtipos histológicos y moleculares; la mediana de supervivencia para el cáncer de mama inflamatorio es de 2,9 meses, el triple negativo es de 4,9 meses, la sobreexpresión de HER2 que recibe trastuzumab es de 11,3 a 26,3 meses, y con receptor hormonal positivo es de 19 a 24 meses.1
Coincido con los autores sobre las debilidades de este trabajo, y que “… cuesta…poder determinar una recomendación estándar sobre síntomas neurológicos”.
Sugerimos las recomendaciones de la National Comprehensive Cancer Network® -NCCN- Versión 1.2020-Marzo 10, 2020.
Considerar la cirugía para metástasis cerebrales:
Resección para el tratamiento del efecto de masa o los síntomas.
Resección para el tratamiento de pacientes con enfermedad sistémica estable o recién diagnosticada u opciones de tratamiento sistémico razonables.
Biopsia si existe duda sobre el diagnóstico del origen de la/s lesión/es en el SNC, y la resección no está planificada.
Considere una revisión multidisciplinaria en la planificación del tratamiento, especialmente una vez que la patología esté disponible.
La radiocirugía estereotáctica puede considerarse para pacientes con buen performance y bajo volumen tumoral general y/o tumores radiorresistentes como el melanoma.2
Si existe un fármaco activo (p. ej.: citotóxico, “dirigido” o inmunomodulador), se puede considerar la prueba de terapia sistémica con buena penetración del SNC en pacientes seleccionados (p. ej., para pacientes con metástasis cerebrales asintomáticas pequeñas de melanoma, o NSCLC con mutación de ALK+ (anaplastic lymphoma kinase, la traducción es mía) o EGFR mutado); es razonable esperar el tratamiento con radiación para ver si la terapia sistémica puede controlar las metástasis cerebrales.3 No existen datos de ensayos clínicos prospectivos que comparen las dos estrategias para evaluar cuál sería el impacto de la radiación retardada en términos de supervivencia o en el retraso del desarrollo del déficit neurológico.
Ignacio Casas Parera
Instituto “Ángel H. Roffo”. Facultad de Medicina. UBA. Ciudad Autónoma de Buenos Aires.
BIBLIOGRAFÍA
- Au K, Meng Y, Suppiah S, Nater A, Jalali R, Zadeh G. Current Management of Brain Metastases: Overview and Teaching Cases, Chapter 6. In New Approaches to the Management of Primary and Secondary CNS Tumors. pp. 121-148. http://dx.doi.org/10.5772/66310
- Yamamoto M, Serizawa T, Shuto T, et al. Stereotactic radiosurgery for patients with multiple brain metastases (JLGK0901): a multi-institutional prospective observational study. Lancet Oncol. 2014;15:387-395.
- Kotecha R, Gondi V, Ahluwalia MS, et al. Recent advances in managing brain metástasis. Version 1. F1000Res. 2018; 7: F1000 Faculty Rev-1772. Published online 2018 Nov 9. doi: 10.12688/f1000research.15903.1


